angsung saja ini langkah demi langkah cara
membuat blogger di Blogspot terbaru :
1. Membuat Email di Gmail.com
Blogger.com sudah di akusisi oleh Google jadi langkah
pertama dalam membuat blog di blogspot ialah kita wajib untuk memiliki
akun GMAIL sebagai email yang digunakan untu daftar di blogger.com.
Walaupun sebenarnya bisa menggunakan email lain tapi percaya deh mending
make GMAIL dari awal.
Cara Membuat Email di Gmail
Daftar GMAIL gratis buka www.gmail.com lalu klik
di pojok kanan atas Create An Account atau Buat Akun
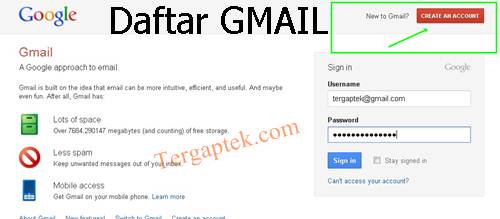 |
| membuat akun
di Gmail.com |
Tinggal isi data data di akun gmail yang akan
dibuat seperti nama, tempat tanggal lahir , password dan lain-lain.
Biasanya dalam membuat email di GMAIL kita perlu
verifikasi lewat nomor handphone jadi usahakan masukan nomor handphone
yang bisa dikirimin sms dari Google untuk verifikasi.
Setelah email di Gmail dibuat baru kita bisa
melanjutkan ke step 2 membuat blog.
2. Daftar di Blogger.com
Setelah membuat email di GMAIL sekarang saatnya
daftar di www.Blogger.com
buka www.blogger.com lalu
klik bagian kanan atas yang bertulisan 'sign up atau daftar'
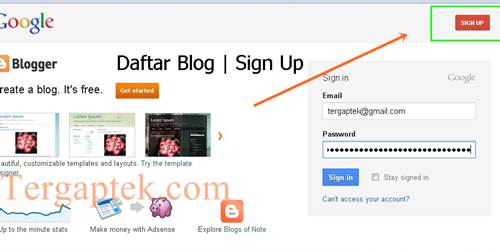 |
| daftar
blogger | Sign Up |
Isi data-data sesuai keinginan :
 |
| Cara bikin blog |
- email : email GMAIL yang kita buat tadi di
tahap 1
- Password : pilihlah password minimal 8
karakter
- Display Name (nama tampilan) : Merupakan
nama yang digunakan sebagai nama kita di akun blog nanti. Misal aku
memilih nama "ayead gaptek" maka nama yang akan muncul ketika aku
posting nanti ialah "posted by
ayead gaptek atau diposting oleh ayead
gaptek"
- Gender (Jenis Kelamin) : pilih kelamin
sesuai kenyataan atau kalau ragu pilih "other atau lainnya"
- Birthday (tanggal lahir) : masukan dengan format
tanggal/bulan/tahun misal jika tanggal lahir 17 agustus 1945 maka yang
dimasukkan = 17/08/1945 jika dalam format bahasa inggris seperti gambar
dibawah maka format tanggalnya ialah bulan/tanggal/tahun
- Word Verification (verifikasi) : masukan karakter
yang terdapat di bawah
- Lalu centang Acceptance of terms (penerimaan
peryaratan)
- Klik Continue / Lanjutkan
Sampai proses diatas sobat
sudah selesai cara membuat akun Blogger, sekarang saatnya membuat
BLOGnya.
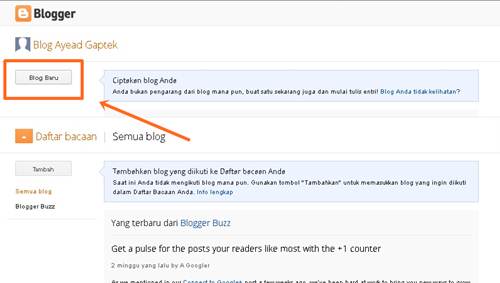
Di akun blogger klik "Blog baru" untuk
membuat blog. Lalu akan muncul halaman untuk memilih Judul, Alamat Blog
dan Template.
 |
| Cara Membuat
Blogger : memilih Judul, Alamat dan template |
Pilih Judul dan Alamat blog.
- Judul digunakan sebagai penama
blog, misal untuk blog ini dulu kuberi judul Blognya Ayead Tergaptek
- Alamat merupakan url alamat blog yang diinginkan
misal alamat blog blogayead.blogspot.com
Saran Gaptek : dalam memilih judul dan nama blog
jangan pilih yang aneh atau susah dieja maupun menggunakan simbol yang
aneh-aneh. Pilih yang mudah diingat orang lain dan tidak membingungkan.
Memilih Template Blog
Ada berbagai template bawaan dari blogger yang
tersedia sobat bisa memilih terserah sesuai dengan yang disuka lalu klik
'Buat
Blog'
Saran Gaptek : Dalam memilih
template blog awal, aku lebih suka dengan template 'AWESOME' karena
lebih terlihat simpel tanpa banyak background gambar. Template yang
namanya 'Simple' justru sebenarnya tidak simpel seperti namanya
karena menggunakan background dalam bentuk gambar sehingga berat untuk
dibuka.
4. Blog Sudah Jadi
Selamat ! sampai disini blog sudah berhasil dibuat,
namun masih kosong. Setelah ini akan ada beberapa hal yang perlu di
setting sebelum melakukan posting.
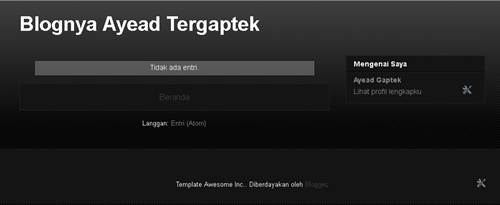 |
| Blog Yang Dibuat
Masih Kosong |
Untuk melihat blog yang baru dibuat bisa langsung
mencoba dengan langsung mengetikan alamat blog yang baru dibuat tadi di
browser contoh : blogayead.blogspot.com
5.
Jangan lupa cek email yang didaftarkan tadi untuk memverifikasi akun
google kita .
Di
email yang kita daftarkan pada tahap 1 nanti akan ada "
Google Email Verification
" buka dan klik link yang ada
di dalam email tersebut
6. Hal Yang Dilakukan Setelah Membuat Blog
Sebelum posting ada beberapa hal yang menurutku
perlu di atur dulu dari blog sobat diantaranya :
Dan Baca Juga recomended : Yang Harus Diketahui Blogger Newbie
7. Blog
Siap Dipakai
Sobat bisa membuat postingan / tulisan baru,
mengedit tampilan
keterangan
:
1.
Membuat Postingan / Tulisan Baru
2. Melihat Postingan / mengedit
post
3.
Mengatur Widget
4. Setting
5. Mengatur Tampilan Template :
warna dan lain-lain
6. Blog Baru, Satu akun blogger bisa digunakan
untuk membuat banyak blog jadi sobat bisa menambah blog lain cukup
dengan 1 akun blogger saja.
Apabila Sobat Merasa
Kesulitan dalam membuat atau mengelola blog, ntuk Info lebih Lanjut
Mengenai Blog Sobat Bisa Membaca Ebook Dari www.Caramembuatblogger.com :
- Rahasia Bagaimana
cara mencari ide yang sedang Hot untuk bahan tulisan blog
Plus minus nantinya
anda akan mempelajari hal2 dibawah ini.
- Rahasia Bagaimana
anda bisa membuat pengunjung anda betah bertahan berjam jam di blog
anda,
- Rahasia
Bagaimana caranya membuat blog anda semirip mungkin dengan orang lain
dengan cara cara sederhana,
- temukan
rahasia widget widget yang sering dipakai oleh para blogger, sangat
berguna sekali untuk mempercantik blog anda
- Rahasia
Bagaimana cara menghipnotis calon pengunjung agar mau mengunjungi blog
anda
- Rahasia
Bagaimana cara agar pengunjung anda menjadi pengunjung yang loyal
terhadap blog anda
- Rahasia
Delapan syarat agar blog anda sempurna
- Rahasia
Belajar bagaimana caranya membuat posting yang menghipnotis
- Rahasia
Prinsip dasar dalam membuat blog yang bagus dan dipercaya
- Rahasia
Bagaimana agar blog anda selalu dicari dan dibutuhkan oleh orang
- Rahasia Dua
prinsip dasar yang harus dimengerti dalam membuat sebuah judul
- Rahasia
Bagaimana cara membuat tulisan header yang di sukai mesin pencari
- Rahasia
Bagaimana cara agar blog anda di sukai mesin pencari
- Rahasia
Bagaimana cara memilih nama blog agar memiliki daya tarik tersendiri
bagi search engine
Dan masih banyak
lagi…
DiKupas dengan sangat detail dalam 4 buah ebook ( Empat buah Ebook ).
Bayangkan semua materi sudah anda genggam ditangan anda, Tidak perlu
lagi mencari kemana mana. Hanya Rp.50.000 anda
mendapatkan segudang manfaat yang luar biasa. bayangkan bila anda
mencari cari tutorialnya di Internet. harga buat beli pulsa modemnya
Rp.100.000 ,-, buat makanan ringan nya minimal Rp.20.000, wahh banyak
banget deh biayanya iya kan... belum lagi kalau kebingungan, trial dan
eror, sangat memboroskan waktu dan tenaga anda bagi anda yang pemula.
Belum lagi ditambah jika ada update produk terbaru, akan langsung
diberikan ke email anda. Investasi sekali bayar seumur hidup. Tolong
sebarkan informasi ini. dengan begitu anda juga membantu teman teman
anda yang kesulitan/awam total dan meringankan mereka. satu lagi, saya
tidak tahu kapan pemilik situs akan menaikan harga atau mungkin menutup
penawaranya